Por Carlos Mendoza Prado, Periodista de Ciencia y Salud, para Mundo IA
Proteínas diseñadas con IA ayudan a rejuvenecer células en cultivo
En un avance que fusiona la vanguardia de la inteligencia artificial con la biología regenerativa, OpenAI y Retro Biosciences han anunciado un trabajo conjunto que utiliza un modelo de IA especializado para proponer cambios en factores clave de reprogramación celular. Este enfoque no se trata de un chatbot conversacional, sino de una herramienta computacional entrenada en vastos conjuntos de secuencias proteicas, literatura biomédica y datos estructurales para sugerir variantes proteicas con mayor potencial de éxito en experimentos de laboratorio. Los resultados preliminares, observados en cultivos celulares in vitro, muestran un aumento en marcadores de pluripotencia y señales de reparación de ADN, sugiriendo un camino hacia protocolos más eficientes para revertir aspectos del envejecimiento celular. Sin embargo, como todo hallazgo preclínico, este requiere validación independiente antes de generar expectativas clínicas.
La reprogramación celular, un concepto que revolucionó la biomedicina desde su descubrimiento por Shinya Yamanaka en 2006, permite devolver células adultas a un estado similar al de las células madre pluripotentes inducidas (iPSCs). Yamanaka identificó cuatro factores de transcripción –OCT4, SOX2, KLF4 y c-MYC, comúnmente abreviados como OSKM– que, al ser introducidos en células somáticas, activan un programa genético que borra las marcas de diferenciación y restaura un potencial pluripotente. Este logro no solo le valió a Yamanaka el Premio Nobel de Medicina en 2012, sino que abrió puertas a aplicaciones en modelado de enfermedades, cribado de fármacos y terapias regenerativas. Imaginen células de la piel de un paciente convertidas en neuronas para estudiar Alzheimer, o en cardiomiocitos para reparar daños cardíacos post-infarto. La idea es elegante en teoría, pero en la práctica enfrenta obstáculos persistentes: eficiencia baja (a menudo por debajo del 1% de células reprogramadas), tiempos prolongados (semanas o meses), variabilidad según el tipo celular de origen y riesgos como inestabilidad genómica o tumorigenicidad.
Aquí es donde entra la priorización computacional asistida por IA. Un modelo de lenguaje grande, adaptado específicamente para el diseño de proteínas, puede explorar espacios de secuencias aminoacídicas que un equipo humano tardaría décadas en cubrir. En lugar de probar variantes al azar en el laboratorio (un proceso costoso y lento), la IA analiza patrones en datos existentes para predecir cuáles mutaciones podrían mejorar la afinidad por el ADN, la estabilidad proteica o la interacción con cofactores. En el caso de este estudio, el modelo se centró en reingeniar SOX2 y KLF4, dos de los factores Yamanaka, generando variantes denominadas RetroSOX y RetroKLF. Estas propuestas no son invenciones aleatorias; surgen de un entrenamiento que integra estructuras cristalográficas, simulaciones moleculares y evidencias de literatura sobre interacciones proteína-ADN.
Según el anuncio publicado en el sitio de OpenAI, el modelo, bautizado como GPT-4b Micro, fue entrenado con un corpus que incluye secuencias proteicas, artículos científicos y datos de plegamiento proteico.
Este enfoque permite que la IA no solo genere secuencias, sino que las priorice basadas en probabilidades de éxito funcional. En experimentos in vitro realizados por Retro Biosciences, estas variantes elevaron la expresión de marcadores de pluripotencia como NANOG y OCT4, y mejoraron parámetros de reparación de ADN, como la activación de vías de respuesta a daños. Células envejecidas, expuestas a estos factores modificados, mostraron rasgos más juveniles en menos tiempo comparado con los OSKM originales. Por ejemplo, se reportó un aumento en la eficiencia de reprogramación y una reducción en el estrés oxidativo, indicadores clave de rejuvenecimiento celular.
Para contextualizar, recordemos que el envejecimiento celular se caracteriza por acumulaciones de daños: telomeros acortados, mutaciones en el ADN, disfunción mitocondrial y pérdida de proteostasis. La reprogramación parcial, una variante del método Yamanaka donde los factores se aplican de manera transitoria, ha mostrado en modelos animales la capacidad de revertir estos marcadores sin llegar a la pluripotencia completa, evitando así riesgos de cáncer. Estudios previos, como los de Juan Carlos Izpisua Belmonte en el Salk Institute, han demostrado en ratones que esta reprogramación in vivo extiende la vida útil y mejora funciones orgánicas. Sin embargo, traducir esto a humanos requiere superar barreras como la entrega selectiva a tejidos y el control preciso de la dosis para evitar efectos off-target.
El rol de la IA en este contexto es transformador porque acelera la fase de descubrimiento. Tradicionalmente, el diseño de proteínas involucra iteraciones manuales: modelado in silico, síntesis, ensayo en células y refinamiento. Con IA, el ciclo se comprime. El modelo de OpenAI, similar a herramientas como AlphaFold de DeepMind para predicción estructural, va un paso más allá al integrar conocimiento biológico para sugerir ediciones funcionales. En palabras de expertos en el campo, esto representa un «cambio de paradigma» donde la máquina actúa como un colaborador hipotético, proponiendo candidatos que el laboratorio valida experimentalmente.
Retro Biosciences, una startup enfocada en longevidad respaldada por inversores como Sam Altman (CEO de OpenAI), busca extender la esperanza de vida saludable en 10 años, y ve en la reprogramación un pilar clave.
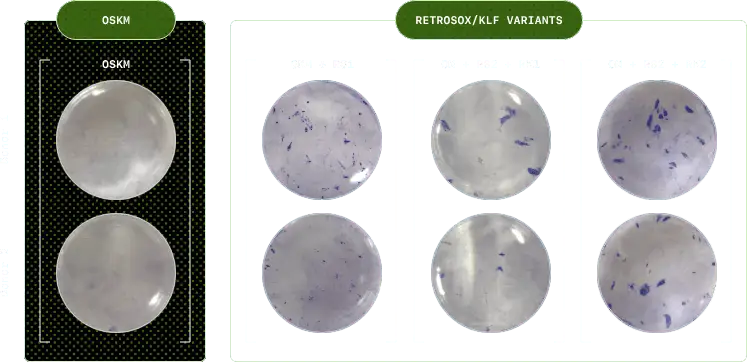
Las colonias púrpuras indican una reprogramación exitosa de células madre; colonias más intensas y numerosas indican una mayor eficiencia.
La tinción con fosfatasa alcalina (AP) de colonias derivadas de fibroblastos al día 10 después de la transducción con las variantes RetroSOX y RetroKLF demuestra una actividad robusta de AP, lo que sugiere que las variantes diseñadas han inducido pluripotencia en las colonias.
Cómo encaja un modelo generativo de proteínas
Detallando los resultados: en cultivos de fibroblastos humanos, las variantes RetroSOX y RetroKLF incrementaron la tasa de células positivas para marcadores pluripotentes en un factor significativo, aunque el anuncio no cuantifica exactamente, fuentes reportan mejoras del orden de 2-5 veces en eficiencia. Además, se observó una potenciación en la reparación de ADN, medida por niveles de γ-H2AX (un marcador de roturas de doble cadena) y activación de enzimas como PARP. Esto sugiere que las proteínas modificadas no solo impulsan la desdiferenciación, sino que mitigan daños acumulados, un doble beneficio para aplicaciones anti-envejecimiento. En términos prácticos, células de donantes ancianos mostraron morfología y proliferación similares a las de donantes jóvenes tras el tratamiento, en un marco temporal reducido.
Pero la prudencia es imperativa. Este es un resultado preclínico, confinado a platos de cultivo. No hay datos in vivo, mucho menos en humanos. La distancia entre un ensayo in vitro y una terapia aprobada es vasta, plagada de desafíos regulatorios y científicos. Por ejemplo, la reprogramación exige controles estrictos de estabilidad genómica: cualquier alteración podría inducir mutaciones oncogénicas. Estudios pasados han mostrado que OSKM puede promover tumores si no se maneja con precisión. Además, la variabilidad interindividual (factores como epigenoma basal o estado inflamatorio) podría modular la respuesta, requiriendo pruebas en múltiples líneas celulares y donantes.
Lo que falta por demostrar es extenso. Primero, reproducibilidad independiente: ¿se replican estos hallazgos en laboratorios ajenos, con protocolos estandarizados? Retro y OpenAI han compartido el modelo y datos, pero validaciones externas son cruciales para descartar sesgos.
Segundo, estabilidad a largo plazo: seguimiento de células reprogramadas por meses para detectar eventos de transformación o senescencia revertida. Tercero, efectos off-target: análisis transcriptómicos y proteómicos para identificar vías no intencionadas activadas. Cuarto, vías de entrega: ¿cómo introducir estos factores en tejidos específicos? Vectores virales como lentivirus son comunes, pero plantean riesgos inmunes; alternativas como mRNA o nanopartículas necesitan optimización. Quinto, documentación regulatoria: datos crudos bajo estándares GMP (Good Manufacturing Practices), criterios de evaluación claros y ensayos de toxicidad. Finalmente, salvaguardas éticas: gobernanza para prevenir usos indebidos, como en biohacking o eugenésia.
Más allá del caso específico, esta colaboración ilustra un giro en el uso de modelos de IA grandes. Lejos de tareas triviales como generar texto, aquí se aplican para hipótesis de diseño biológico. El valor radica en priorizar candidatos viables, ahorrando recursos en fases tempranas de I+D. Imaginen extender esto a otros dominios: diseño de enzimas para degradar plásticos, anticuerpos contra patógenos emergentes o moduladores de vías metabólicas en cáncer. Retro Biosciences, fundada en 2021 con financiación de Altman, se posiciona en la intersección de IA y longevidad, junto a jugadores como Calico (de Alphabet) o Altos Labs.
El impacto potencial es transversal. Protocolos más eficientes acortarían cronogramas de investigación, reduciendo costos y facilitando colaboraciones interinstitucionales. En medicina regenerativa, podría acelerar terapias para enfermedades como Parkinson o diabetes tipo 1, donde iPSCs derivadas del paciente evitan rechazo inmune. En longevidad, contribuiría a intervenciones que retrasen el envejecimiento sistémico, como la eliminación de células senescentes o restauración de tejidos. Sin embargo, el hype debe moderarse: avances como este son ladrillos en un edificio complejo, no la estructura completa.
En un panorama más amplio, consideremos la evolución de la reprogramación. Desde Yamanaka, refinamientos han incluido factores químicos (evitando genes virales) y reprogramación in vivo directa. Trabajos como el de Ocampo et al. en 2016 mostraron rejuvenecimiento en ratones progeroides mediante OSKM cíclico. Ahora, con IA, se añade precisión molecular. Expertos como Alejandro Ocampo destacan que «la IA puede desbloquear variantes que la evolución no priorizó, pero la biología impone límites». Desafíos persistentes incluyen escalabilidad: producir suficientes células para trasplantes, y equidad: asegurar acceso global a estas tecnologías.
Desde la óptica económica, el mercado de biotecnología regenerativa se proyecta en cientos de miles de millones para 2030. Inversiones en IA para bio-diseño, como las de OpenAI en Retro, podrían catalizar esto, pero requieren marcos regulatorios robustos. Agencias como la FDA exigen fases I-III con datos sólidos de seguridad y eficacia. En Europa, la EMA enfatiza evaluaciones de riesgo-beneficio para terapias avanzadas.
Éticamente, surge el debate: ¿deberíamos perseguir la longevidad extrema? Críticos argumentan que extender la vida sin abordar desigualdades sociales amplificaría brechas. Proponentes ven un imperativo moral en combatir el envejecimiento como enfermedad. Gobernanza global, como la propuesta por la OMS para IA en salud, es esencial.
Este estudio demuestra que la IA puede asistir en el rejuvenecimiento celular al proponer variantes de factores Yamanaka con mejor desempeño in vitro. Es una prueba de concepto prometedora, pero preclínica. Lo siguiente es replicar en entornos independientes, perfilar seguridad exhaustivamente y verificar escalado in vivo. Si estos pasos confirman los beneficios, la sinergia entre IA y biología de reprogramación podría acortar dramáticamente los tiempos de investigación, abriendo rutas más fiables hacia aplicaciones futuras en longevidad y regeneración. Mientras tanto, la comunidad científica debe equilibrar entusiasmo con rigor, recordando que el verdadero progreso surge de la validación, no del anuncio inicial.