Por Carlos Mendoza Prado, Periodista de Ciencia y Salud, para Mundo IA
IA Agentica Desentraña Conexiones Ocultas Entre Enfermedades Mediante Análisis Transcriptómico Avanzado
En un mundo donde la inteligencia artificial está revolucionando la forma en que entendemos la salud humana, un equipo de investigadores de la Universidad de Illinois Urbana-Champaign ha presentado un estudio innovador que utiliza IA agentica para mapear relaciones entre enfermedades a través de patrones genéticos. El paper, titulado «Discovery of Disease Relationships via Transcriptomic Signature Analysis Powered by Agentic AI», explora más de 1,300 pares de condiciones médicas analizando datos transcriptómicos masivos. Este enfoque no solo confirma comorbilidades conocidas, como las entre diabetes y problemas cardíacos, sino que revela vínculos moleculares inesperados, como el que conecta la enfermedad de Alzheimer con el melanoma ocular. La promesa es clara: al pasar de descripciones basadas en síntomas a mecanismos biológicos profundos, esta tecnología podría acelerar el desarrollo de tratamientos personalizados, el repurposing de fármacos existentes y avances en la medicina preventiva, todo ello con un enfoque accesible y automatizado que pone el poder de la IA en manos de investigadores cotidianos.
Un marco de IA agentica llamado GenoMAS procesa automáticamente datos genéticos de miles de muestras, construyendo redes de similitud que destacan cómo enfermedades aparentemente desconectadas comparten vías moleculares, ofreciendo nuevas hipótesis para la investigación médica.
El estudio identifica moduladores como la obesidad y la hipertensión que influyen en estas conexiones, sugiriendo oportunidades para reutilizar terapias en trastornos complejos como el autismo, y pone todos los datos y códigos a disposición pública para fomentar colaboraciones globales.
La apuesta y el contexto
Imagina por un momento que las enfermedades no son entidades aisladas, definidas solo por los síntomas que vemos en una consulta médica, sino redes interconectadas de procesos biológicos que se entretejen en lo profundo de nuestras células. Esta es la visión que impulsa el nuevo paper publicado en arXiv por Ke Chen y Haohan Wang, dos investigadores de la Universidad de Illinois Urbana-Champaign. Su trabajo, titulado «Discovery of Disease Relationships via Transcriptomic Signature Analysis Powered by Agentic AI», representa un paso adelante en la integración de la inteligencia artificial con la genómica, específicamente en el campo de la transcriptómica, que estudia cómo los genes se expresan en diferentes condiciones.
Lo que ocurrió es que los autores desarrollaron y aplicaron un sistema de IA agentica llamado GenoMAS para analizar un vasto conjunto de datos llamado GenoTEX. Este dataset es un tesoro de información biológica: incluye más de 150,000 muestras de tejidos y células humanas, provenientes de 132 enfermedades diferentes y 911 cohortes de estudio. Cada cohorte representa un grupo de muestras recolectadas bajo condiciones específicas, como la presencia de factores de riesgo como edad avanzada, sexo, obesidad o comorbilidades como hipertensión. El objetivo era examinar 1,384 pares posibles de enfermedad-condición, buscando patrones en cómo los genes se activan o desactivan en cada escenario.
Utilizando GenoMAS, que actúa como un asistente inteligente autónomo, el equipo automatizó el proceso entero: desde la limpieza y normalización de los datos hasta el cálculo de similitudes genéticas y el análisis de vías biológicas. El resultado fue la construcción de una red de similitud que conecta estas enfermedades de maneras inesperadas. Por ejemplo, el estudio confirmó agrupamientos lógicos, como enfermedades nerviosas que se agrupan juntas, pero también desenterró enlaces cruzados, como entre la espondilitis anquilosante (una forma de artritis) y la osteoporosis, o entre la hemochromatosis (acumulación de hierro) y el cáncer de hígado.
Pero lo más noticioso es la identificación de cómo condiciones de fondo, como la obesidad o la hipertensión, modulan estas similitudes. En 11 de los 20 pares con las puntuaciones más altas de similitud, la hipertensión jugaba un rol amplificador, sugiriendo que controlar estos factores podría mitigar riesgos en cánceres y trastornos musculoesqueléticos. Además, el paper aplica este marco a un caso práctico: el trastorno del espectro autista (ASD, por sus siglas en inglés), revelando similitudes con osteoporosis y diabetes tipo 1, lo que abre puertas a repurposing de fármacos como estatinas o agonistas PPARγ.
Todo esto se hizo con un compromiso con la transparencia: el código fuente de GenoMAS, los datos procesados y las visualizaciones de las redes están disponibles en GitHub, invitando a la comunidad científica a replicar, expandir o criticar el trabajo. Este lanzamiento público no es menor; en un campo donde los datos a menudo se guardan bajo llave por razones competitivas, esta apertura acelera el progreso colectivo. El paper llega en un contexto de explosión de datos biomédicos: con biobancos como UK Biobank o All of Us generando terabytes de información genómica, herramientas como GenoMAS son esenciales para extraer valor sin ahogarse en la complejidad.
Desde una perspectiva periodística, este desarrollo destaca en un año donde la IA agentica (sistemas que no solo responden a comandos, sino que planifican y ejecutan tareas complejas de forma independiente) ha ganado tracción. Empresas como OpenAI y Google han invertido en agentes para tareas creativas y científicas, pero aplicaciones en biomedicina como esta demuestran su potencial real para resolver problemas del mundo real. Los autores, Chen y Wang, no son novatos; su laboratorio ha publicado previamente sobre IA biológicamente informada, y este paper construye sobre eso, posicionándolos como pioneros en la intersección de machine learning y salud.
En resumen, lo que pasó es una demostración de cómo la IA puede actuar como un detective molecular, conectando puntos que los humanos solos tardarían años en ver. Esto no es solo académico; podría influir en cómo diagnosticamos y tratamos enfermedades en el futuro cercano, especialmente en una era post-pandemia donde entender comorbilidades es clave para la resiliencia sanitaria global.
El método, de punta a punta
Para entender cómo se logró este avance, hay que desglosar el método paso a paso, manteniendo un nivel accesible para quien no es experto en genómica o IA. El corazón del estudio es GenoMAS, un framework de IA agentica multi-agente. ¿Qué significa «agentica»? Piensa en ella como un equipo de robots inteligentes que trabajan juntos: cada «agente» maneja una tarea específica, como limpiar datos o calcular estadísticas, y se coordinan para lograr un objetivo mayor sin necesidad de supervisión constante. A diferencia de modelos de IA como ChatGPT, que responden a prompts uno por uno, los sistemas agenticos planifican secuencias de acciones, ajustándose sobre la marcha.
Los autores comenzaron con el dataset GenoTEX, un benchmark diseñado específicamente para probar asociaciones gen-enfermedad bajo condiciones variables. GenoTEX no es cualquier base de datos; es un conjunto curado que integra expresiones génicas de fuentes públicas como GEO (Gene Expression Omnibus), normalizadas para comparabilidad. Cada muestra incluye metadatos: por ejemplo, si el paciente tenía obesidad (definida por IMC >30) o hipertensión. En total, 132 enfermedades cubren un amplio espectro, desde cánceres hasta trastornos neurológicos, con un promedio de 18,000 genes medidos por muestra.
El pipeline de GenoMAS inicia con preprocesamiento automático. Los datos crudos a menudo tienen ruido –valores faltantes, variabilidad técnica–, así que el agente de limpieza aplica normalización (el paper no detalla el método específico) y controles de calidad. Luego, para cada par enfermedad-condición (como Alzheimer con obesidad), se usa regresión Lasso. Lasso es una técnica estadística que selecciona genes relevantes minimizando un modelo lineal con penalización, identificando aquellos con coeficientes |β| > 0.05 como significativos. Esto genera listas de genes «firma» para cada par, capturando cómo la condición de fondo altera la expresión en la enfermedad principal.
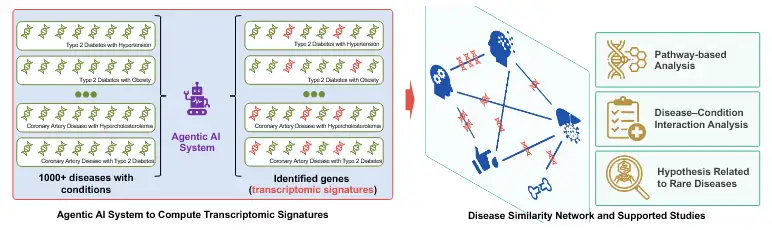
Fig. 1 Análisis con IA agentica de datos transcriptómicos para identificar firmas transcriptómicas y la red de enfermedades construida a partir de esas firmas.
A continuación, para construir la red de similitud a nivel de genes, GenoMAS calcula solapamientos pairwise entre estas listas usando pruebas hipergeométricas bidireccionales. Esta prueba evalúa si el overlap es mayor al esperado por azar, corrigiendo por múltiples comparaciones con Benjamini-Hochberg para mantener FDR ≤ 0.05. De miles de posibles enlaces, emergen alrededor de 65,000 significativos, reducidos a 1,293 tras filtrar redundancias y auto-enlaces. La red se construye con la biblioteca Python NetworkX, donde nodos son pares enfermedad-condición y aristas pesadas por -log10(FDR), indicando fuerza de similitud. Visualizaciones usan layouts de muelle para agrupar nodos similares.
Pero el verdadero ingenio está en el análisis de vías biológicas, que añade interpretabilidad. Para los 1,293 pares genéticos significativos, GenoMAS realiza enriquecimiento de vías usando seis bases de datos estándar: Gene Ontology (GO) para procesos biológicos, Reactome para reacciones, KEGG para metabolismos, bases de factores de transcripción, miRNA y ontología de fenotipos humanos. Se priorizan términos de alto nivel para evitar ruido granular. Para cada par, se identifican vías compartidas, y se computa un score de similitud como la suma de log((1 – p1k) × (1 – p2k)) para cada vía k común, donde p son p-values de enriquecimiento. Solo scores positivos se retienen, resultando en 1,060 combinaciones.
La red de vías es un grafo no dirigido, con nodos coloreados por categorías del ICD-10-CM (el sistema internacional de clasificación de enfermedades) y aristas escaladas por scores. Para validación, se compara con taxonomías clínicas: un heatmap muestra similitudes promedio dentro y entre capítulos ICD, confirmando coherencia interna pero también destacando cruces en los que algunos capítulos exhiben mayor similitud con otros capítulos que consigo mismos (por ejemplo, subtipos de los capítulos 2 y 3 con el capítulo 13). Además, para hipótesis iniciales, se usa GPT-4o para generar explicaciones plausibles de enlaces, aunque los autores enfatizan que esto es exploratorio.
Todo el proceso es reproducible: el código en GitHub incluye scripts para descargar GenoTEX, ejecutar GenoMAS y generar figuras. Los autores usaron entornos estándar de Python (pandas para datos, scipy para estadísticas y matplotlib para plots). El paper no especifica requisitos de hardware; el pipeline es reproducible con herramientas comunes, lo que sugiere una accesibilidad amplia.
En esencia, lo hicieron combinando automatización IA con rigor científico, creando un pipeline que escala análisis que manualmente tomarían meses. Esto no es solo técnico; es un modelo para futuras investigaciones donde la IA actúa como co-investigador.
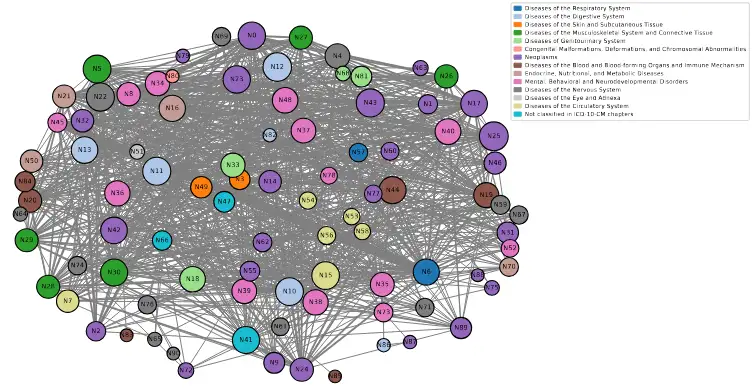
Fig. 2 Red de similitud a nivel de vías. Cada nodo representa un par enfermedad-condición, coloreado según la categoría ICD-10-CM. Las aristas indican un solapamiento estadísticamente significativo en las vías enriquecidas. Tanto el grosor como la longitud de cada arista reflejan la fuerza de la similitud: una mayor similitud a nivel de vías se traduce en aristas más cortas y más gruesas. El tamaño del nodo refleja la centralidad de grado. Aunque muchos nodos están conectados, esta visualización está diseñada para resaltar la fuerza de la similitud más que la mera presencia de conexión.
Hallazgos que conectan los puntos
Los logros del estudio son multifacéticos, combinando validación de conocimiento existente con descubrimientos novedosos. Primero, la red de similitud a nivel de genes (construida de 1,293 pares) valida la estructura del ICD-10-CM. Por ejemplo, enfermedades del capítulo 6 (sistema nervioso) se agrupan fuertemente, con similitudes altas en pares como enfermedad de Canavan y epilepsia, compartiendo genes relacionados con percepción sensorial y receptores GPCR. Similarmente, capítulos 9 (circulatorio) y 13 (musculoesquelético) muestran bloques diagonales en el heatmap de Figura 2, indicando coherencia interna.
Pero los hallazgos más emocionantes son los enlaces cruzados. El heatmap revela off-diagonales fuertes y, en varios casos, capítulos que muestran su mayor similitud con otros capítulos (por ejemplo, subtipos de los capítulos 2 y 3 con el 13), sugiriendo mecanismos compartidos entre neoplasias, trastornos sanguíneos-inmunes y afecciones musculoesqueléticas. La red basada en vías (Figura 3) visualiza esto: nodos grandes para enfermedades centrales como cáncer de próstata, aristas gruesas para similitudes altas. Ejemplos conocidos incluyen cáncer de estómago y úlcera péptica, unidas por vías gastrointestinales.
Descubrimientos novedosos abundan. Para espondilitis anquilosante y osteoporosis, se identifican genes como AAMDC y ABCB1, enriquecidos en metabolismo lipídico e inflamación crónica. Esto sugiere que inflamación ósea en espondilitis podría exacerbar pérdida ósea en osteoporosis. Otro: hemochromatosis y cáncer de hígado, con genes como AADAT y A1BG en vías de aminoácidos e inmunidad innata, apuntando a sobrecarga de hierro como trigger oncológico. Gaucher (acumulación lisosomal) y carcinoma renal cromófobo comparten A1BG y A4GNT en matriz extracelular, insinuando disfunción lisosomal común.
Un foco clave es la modulación por condiciones de fondo. Obesidad amplifica similitudes en celiaquía y carcinosarcoma uterino vía glicoesfingolípidos, implicando alteraciones metabólicas. Hipertensión, presente en 11 de top 20 pares, modula leucemia mieloide aguda y osteoartritis mediante ECM y glucocorticoides, sugiriendo estrés vascular como factor común.
En el caso de ASD, una subred (Figura 5) conecta con osteoporosis (genes AADAC, ABCF3 y ABCA7; vías de lípidos) y diabetes tipo 1 (genes AADAT, ABCD1 y AATF; oxidación de ácidos grasos), lo que abre puertas a repurposing de fármacos como estatinas o agonistas PPARγ.
Figura 4 detalla Alzheimer y melanoma ocular: catabolismo de aminoácidos y β-oxidación, con p-values <10^-5, indicando estrés oxidativo mitocondrial compartido. Figura 1 resume el pipeline.
En total, lograron una red interpretable que genera hipótesis testables, con 1,060 combinaciones validadas, destacando el poder de IA para descubrimientos a escala.
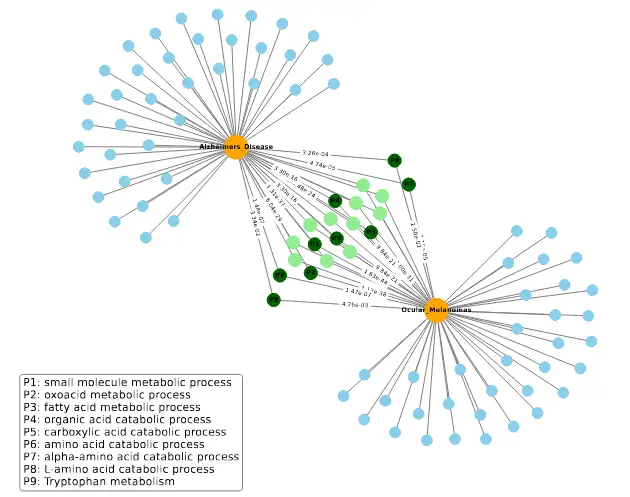
Fig. 3 Vías transcriptómicas compartidas entre la enfermedad de Alzheimer y el melanoma ocular. El gráfico muestra las 50 vías enriquecidas más significativas en cada enfermedad. Los nodos azules representan vías altamente enriquecidas pero no compartidas. Los nodos verdes indican las vías compartidas por ambas enfermedades, destacándose en verde más oscuro aquellas potencialmente relevantes para la comorbilidad, como el catabolismo de aminoácidos y la β-oxidación. Las etiquetas de las aristas reflejan la significancia de las vías (valores p), y la longitud de las aristas se ajusta en función de dicha significancia.
Impacto clínico y horizonte inmediato
Este trabajo importa porque cambia el paradigma de cómo vemos las enfermedades. Tradicionalmente, clasificaciones como ICD se basan en síntomas y anatomía, pero ignoran mecanismos moleculares. Al mapear similitudes transcriptómicas, el estudio revela que condiciones «distantes» comparten raíces biológicas, permitiendo predicciones de comorbilidades. Por ejemplo, saber que hipertensión modula enlaces cáncer-óseo podría guiar screenings preventivos.
En medicina personalizada, implica tratamientos tailor-made: si ASD comparte vías con diabetes, fármacos para uno podrían probarse en el otro, acelerando repurposing. Esto ahorra billones en desarrollo farmacéutico; repurposing cuesta fracciones comparado con nuevos compuestos.
Para longevidad, entender moduladores como obesidad ayuda en intervenciones anti-envejecimiento, donde comorbilidades aceleran declive. En salud pública, informa políticas: campañas contra hipertensión podrían reducir riesgos en múltiples enfermedades.
La IA agentica democratiza: GenoMAS automatiza análisis complejos, accesible para labs pequeños. Transparencia fomenta colaboración, alineado con open science.
Efectos potenciales: en oncología, enlaces como hemochromatosis-hígado podrían llevar a terapias dirigidas. En neurología, Alzheimer-melanoma sugiere enfoques antioxidantes comunes. Globalmente, con datasets crecientes, herramientas como esta escalan descubrimientos, potencialmente salvando vidas al anticipar epidemias de comorbilidades.
Preguntas que aún están sobre la mesa
A pesar de sus fortalezas, el estudio es exploratorio y deja preguntas abiertas. Principalmente, ¿son estos enlaces causales o solo correlacionales? Validación experimental (ensayos in vitro, modelos animales) es esencial para confirmar mecanismos. Por ejemplo, manipular genes como A1BG en células podría probar si alteran fenotipos.
Bias en datasets: GenoTEX, aunque amplio, podría sesgar hacia poblaciones occidentales, limitando generalizabilidad a grupos étnicos diversos. Variabilidad en tamaños de cohortes (algunas con pocas muestras) podría inflar FDR.
Limitaciones en IA: GenoMAS automatiza, pero errores en preprocesamiento (e.g., normalización inadecuada) podrían propagarse. Uso de GPT-4o para hipótesis es preliminar; necesita revisión humana experta.
No aborda confounders como interacciones gene-ambiente o longitudinalidad: ¿cambian similitudes con tiempo? Inferencia causal, usando métodos como Mendelian randomization, falta.
Futuros trabajos: integrar multi-ómicos (proteómica, metabolómica) para redes más robustas. Validación clínica en cohortes grandes como UK Biobank. Ética: privacidad en datos genéticos debe priorizarse.
En suma, mucho por saber, pero el paper establece base sólida para investigaciones subsiguientes.
Una frase para guardar
«Al examinar las vías biológicas compartidas, exploramos posibles mecanismos moleculares subyacentes, ofreciendo hipótesis funcionales que van más allá de las taxonomías basadas en síntomas.»
Glosario a mano
Transcriptómica: Análisis de la expresión de todos los genes en un tejido o célula en un momento dado, revelando cómo responden a enfermedades o condiciones.
IA Agentica: Sistemas de IA que actúan de forma autónoma, planificando y ejecutando tareas complejas como un agente humano, en este caso para análisis genómicos.
Firma Transcriptómica: El patrón único de genes activos o inactivos asociado a una enfermedad bajo una condición específica, como con obesidad.
Enriquecimiento de Vías: Método estadístico para determinar si un grupo de genes se asocia más de lo esperado con procesos biológicos conocidos, como metabolismo.
Repurposing Terapéutico: Estrategia para usar fármacos aprobados para nuevas enfermedades basadas en similitudes moleculares, reduciendo tiempo y costo de desarrollo.
ICD-10-CM: Código internacional para clasificar enfermedades por síntomas, órganos y causas, usado aquí para validar las redes de similitud.
Este estudio con IA agentica ilustra un futuro donde la tecnología desentraña los misterios moleculares de la salud, convirtiendo datos abrumadores en conocimientos que podrían extender vidas y mejorar tratamientos. Si se valida, podría marcar el inicio de una era de medicina verdaderamente conectada, donde las enfermedades no se combaten aisladamente, sino como parte de un ecosistema biológico integral.